В конце августа «Ежедневник» выпустил в двух частях большое расследование по поводу корейской вакцины Эупенты, после введения которой умер ребенок в Ганцевичском районе. После этого произошло многое – брифинг Минздрава, где журналистам не дали задать вопросы, началось расследование СК, президент поручил председателю СК взять дело под личный контроль. А 7 сентября Минздрав опубликовал пресс-релиз, в котором указано, что «Міністэрства аховы здароўя атрымала адказ ад кампаніі LG Chem» по поводу всей ситуации. По мнению «Ежедневника», появилось еще больше вопросов.
Как корейцы быстро меняют сертификаты
После гибели ребенка представители компании LG Chem пообещали разобраться в деле и официально озвучили первую информацию о том, как широко применяется вакцина, и что десятки миллионов использованных доз не дали ни одного серьезного побочного эффекта. Корейцы показали сертификат №5115 от 27.05.2014, выданный Ministry of Food and Drug Safety.
В своей первой части расследования «Ежедневник» указал, что сертификат не может быть действительным и либо является подделкой, либо неким другим документом. Дело в том, что клинические испытания вакцины закончились в апреле 2015 года, поэтому до их окончания сертификат о безопасности лекарственного средства выдать не могли. А на сайте Pharma Korea, который действует от имени Ministry of Food and Drug Safety, вакцина Эупента до сих пор находится в разделе научных разработок, не получившей регистрации в Южной Корее.
В своем последнем ответе представители компании LG Chem указали, что сайт Pharma Korea не отражает текущее состояние регистраций и закрыт с февраля 2018 года: «Официальный веб-сайт Министерства по безопасности продуктов и лекарств (Ministry of Food and Drug Safety, https://ezdrug.mfds.go.kr, также известный как KFDA) располагает верную и актуальную информацию о том, что вакцина Эупента зарегистрирована в Корее». Также корейцы прислали копию сертификата фармацевтического продукта Эупенты в 2015 г. (старая версия) и 2018 г. (обновленная версия). Минздрав не показал эти документы общественности.
Журналист «Ежедневника» задается вопросами: «Что за сертификат от 2014 года был привезен корейцами изначально? Почему о нем тут же забыли, как только «Ежедневник» написал, что он не может являться действительным? Как на этом фоне в принципе можно доверять двум новым сертификатам, присланным взамен разоблаченного, тем более, без номеров и конкретных дат выдачи?»
О «конфиденциальной информации» по мнению Минздрава
Журналист отправил в Минздрав запрос с просьбой предоставить для обозрения указанный сертификат. В ведомстве сначала пообещали это сделать, но через несколько дней ответили отказом: «В сертификате или в приложении к нему всегда указана пропись (полный состав) готового продукта – эта информация подробно раскрывает количественный состав ингредиентов в продукте. Эти сведения являются конфиденциальными, и конечно, всегда найдутся охотники получить такую информацию о конкурентах, чтобы использовать ее в своих целях. Эта информация может быть представлена только с согласия держателя регистрационного удостоверения, или, если продукты не зарегистрированы – заявителя на получение сертификата. Безусловно, распространение такой информации (фактически – производственной рецептуры) без согласия держателя регистрационного удостоверения запрещено и грозит судебными исками к стороне, нарушившей конфиденциальность».
Все сертификаты, подтверждающие качество и безопасность продукта – это публичные документы. Многие производители, в том числе и лекарственных средств, вывешивают такие документы на своем сайте, чтобы любой желающий мог с ними ознакомиться. «Количественный состав ингредиентов», по словам журналиста, – это обязательная информация, которая должна указываться на упаковке лекарственного средства и в инструкции. Например, французский аналоги Эупенты указал весь состав.

Любая контрольно-аналитическая лаборатория с легкостью выяснит количественный состав любого препарата. Секрет в технологии. К тому же, утверждает журналист, ничто не мешало Минздраву удалить «секретную информацию», но предоставить все остальное.
Найти сложно, но можно
Дальше «Ежедневник» занялся поисками сертификата: «Официальный сайт Ministry of Food and Drug Safety, на который ссылаются корейцы, располагается немного по другому адресу. Именно на него ссылаются все авторитетные источники, в том числе и ВОЗ. На этом сайте мы нашли информацию о выпускаемых компанией LG Life Sciences продуктах. Запись датирована мартом 2016 года и среди разрешенных к выпуску продуктов компании нет Eupenta. Получается, что минимум на эту дату вакцина еще не была зарегистрирована в Южной Корее». По крайней мере в английской версии сайта про LG Chem информации нет.
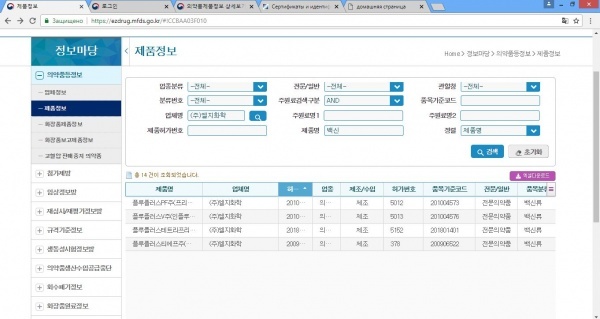
Журналист поискал еще сайты: «А вот совсем другой сайт. Это домен четвертого уровня того же официального сайта Ministry of Food and Drug Safety. Но на вся информация дана исключительно на корейском языке. Практически все поисковые запросы можно производить только зарегистрированным пользователям, которыми могут быть исключительно жители Южной Кореи и представители корейских компаний. Может быть, именно на это и рассчитывали представители корейской компании, давая ссылку на данный домен, по которому практически невозможно что-либо проверить? Впрочем, мы тоже кое-что можем».
Сайт содержит информацию о выдаче сертификатов этим ведомством. Также тут есть информация о проведении клинических испытаний лекарств и о всех негативных реакциях и запретах. Но это все доступно только зарегистрированным пользователям. «Ежедневнику» удалось найти только одну открытую форму запроса, но и по нему, если ввести название вакцины Eupenta, ничего не выдавалось, поскольку наименование лекарственного средства должно быть на корейском. Переводчик не помог, поэтому журналист решил ввести на корейском запрос 'вакцина' (백신). В итоге получил 169 записей.
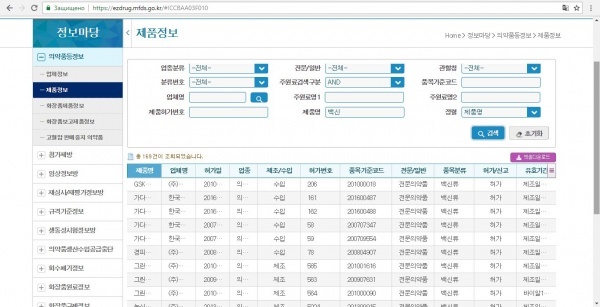
Нашелся сертификат №5115 от 27.05.2014, который корейцы предоставили первым, когда все только начиналось.
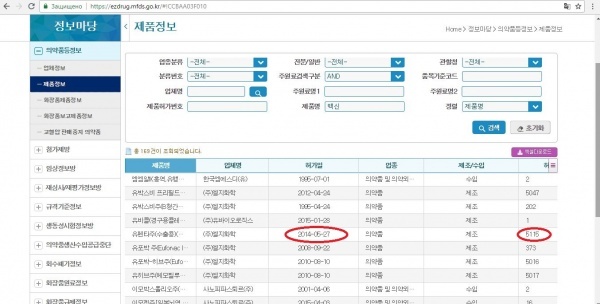
Журналист скачал данные и кинул их в переводчик. Результат: «Eupenia (для экспорта) (адсорбционная дифтерия, столбнячный токсоид, коклюш, вакцина против гепатита B (рекомбинантный геном) и комбинированная вакцина против конъюгата нетоксичного / столбнячного токсоида Haemophilus influenza). LG Chemical Co., Ltd. 2014-05-27. Производство лекарств 5115 201402394. Ветеринарная лекарственная вакцина. Разрешена 36 месяцев с даты изготовления».
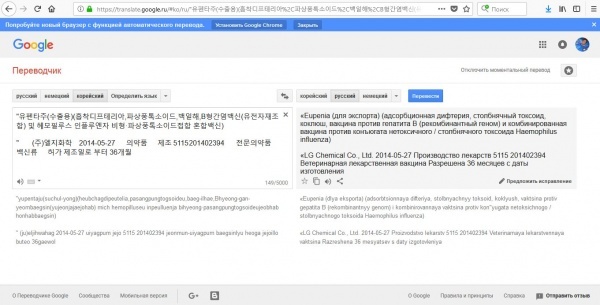
«Официальный перевод, сделанный одним из бюро, дал несколько иной вариант, но все равно, совершенно очевидно, что это не регистрация в Южной Корее. Например, в графе лицензия/регистрация четко указано «лицензия». То есть это лицензия (разрешение), причем, на экспорт, для которого нет необходимости проходить какие-то испытания и регистрацию в Южной Корее. Тут, судя по всему, регулирующий орган исходил из той позиции, что регистрация будет получаться в той стране, куда препарат экспортиртируют», – пишет «Ежедневник».
Выходит, корейцы в качестве подтверждения безопасности вакцины показали лицензию на экспорт вместо регистрационного удостоверения?
Журналист уверен, что Минздрав Беларуси знал об этом нюансе, потому что после гибели ребенка должен был «самым внимательным образом изучить документ и проверить его», и именно поэтому не показывает его общественности. «Об этом говорят и другие факты. Как только «Ежедневник» указал, что сертификат №5115 не может являться подтверждением безопасности вакцины Эупента, а к делу подключились СК и президент, тут же был опубликован другой релиз, в котором о первом сертификате не упоминается и словом (возможно, для того, чтобы СК не изъял его для проверки), зато появились два новых сертификата. При этом чиновники Минздрава даже не поинтересовались у корейцев, почему они вдруг заменили сертификат и как могут пояснить предоставление первого».
Благодаря сертификату №5115 журналист получил название препарата и название фирмы на корейском, но так и не смог найти два новых сертификата на сайте: «Введя название фирмы LG Chem на корейском ((주)엘지화학) мы получили 130 записей, касающихся выдачи каких-либо разрешений или сертификатов указанной компании. Но среди них только одна запись (№5115) касалась вакцины Эупента».
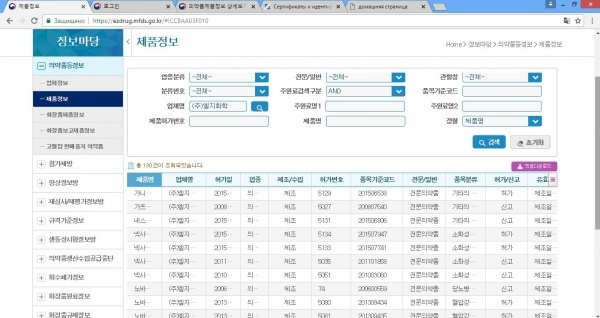
Мы сузили параметры поиска и ввели не только название компании, но и слово 'вакцина'. В итоге получили 14 записей, среди которых вообще нет ни одной, датированной 2015 годом. Но есть одна от 2018 года под №5152, но это опять же не Эупента. Поэтому к корейской компании вновь возникают вопросы, что за новые сертификаты они предоставили.
Производственная площадка, преквалификация ВОЗ и регистрации
В официальном заявлении представитель LG Chem указал, что вакцина Эупента изначально выпускалась на производственной площадке Osong, поэтому неверны выводы «Ежедневника», что в 2016 году производство было перенесено с завода Iksan на Osong (что автоматически аннулирует преквалификацию ВОЗ). Корейцы также указали, что преквалификация ВОЗ проводится только после трех фаз клинических испытаний. Якобы это подтверждается серией технических докладов ВОЗ 978 (ВОЗ TRS).
Журналисты не нашли эти доклады на сайте ВОЗ, поэтому взяли описание требований преквалификации. Касаемо клинических испытаний там есть только одно требование: «результаты тестов на биоэквивалентность (клинических испытаний, проводимых на здоровых добровольцах), если только это требование не снято». Испытания на здоровых добровольцах – это и есть первая фаза, но даже это требование может быть снято.
Также во время подготовки первого расследования «Ежедневник» послал в Минздрав запрос, попросив пояснить, на основании каких сертификатов, подтверждающих безопасность вакцины Эупента, препарат был ввезен в Беларусь и запущен в массовое использование. В ответе говорится о том, что вакцина получила преквалификацию ВОЗ и даются интернет-ссылки на соответствующий протокол обследования производственной площадки и на сам документ преквалификации. Вот протокол обследования (PDF) завода Iksan на предмет выпуска трех препаратов (Eupenta, Euvax, Euforvac).
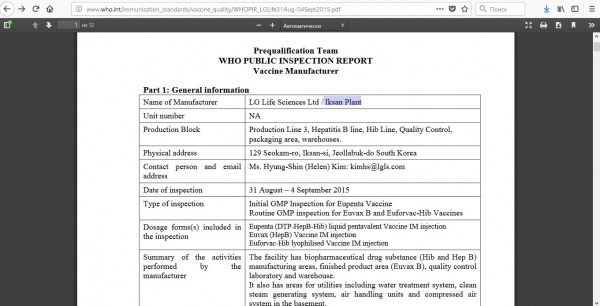
Журналист утверждает, что Минздрав и корейцы «по сути опровергают сами себя». Он дает пример на материалы в корейских СМИ – например, здесь. В нем представитель компании LG Life Sciences, которая тогда и являлась производителем Эупенты, рассказывает, что «компания инвестировала около 260 миллиардов вон в расширение своего завода по производству вакцин в провинции Осонг, провинция Северная Чунчхон», а также «увеличенный завод будет производить Eupenta вместе с Euvax B, начиная со следующего года» (то есть с 2016 года – Прим.). А протокола обследования новой производственной площадки в Osong после 2016 года, откуда вакцина и поставлялась в Беларусь, у компании LG Chem, как и у ВОЗ, нет. Либо Минздрав его не предоставляет.
О странах, где Эупента зарегистрирована
Как указали корейцы в своем письме, Эупента зарегистрирована в девяти странах: Южной Кореей, Узбекистаном, Пакистаном, Шри-Ланки, Республики Союз Мьянма, Сирией, Эфиопией, Филиппинами, Демократической Республикой Конго. Список говорит сам за себя.
О Южной Корее все сказано выше. Из остальных стран «ни одна не входит в список с высокими регуляторными требованиями, на которые так любит ссылаться Минздрав», как утверждает журналист. «При этом практически все – это классический контингент ВОЗ, куда лекарства поставляются в рамках преквалификации. Несколько лет назад в Пакистане были подозрения на эпидемию, а потом при помощи ВОЗ выяснилось, что это местный производитель лекарственных средств допустил передозировку одного из компонентов. Умерли десятки людей. При этом в Пакистане не оказалось даже лаборатории, чтобы провести исследования подозреваемого препарата», – пишет он.
В рамках программ ООН обеспечение лекарствами неблагополучных стран происходит по следующей схеме: если в стране есть соответствующий регулирующий орган, то он производит регистрацию лекарственного средства на основе преквалификации ВОЗ. Если в стране нет такого органа, то лекарства ввозятся и вовсе без какой-либо регистрации в стране. «Ежедневник» делает вывод, что «предоставленный корейцами список ровным счетом ни о чем не говорит, так как речь шла о регистрации в странах с требованиями, аналогичными белорусским, например, в странах ЕС, в США, России, Канады, Японии, Украины. Там Эупента нигде не зарегистрирована, хотя попытки были».
Отдельно журналис затрагивает Узбекистан. «О нем, кстати, говорил, и представитель ООН, утверждая, что там законодательство аналогичное беларускому. Мы зашли на сайт Минздрава Узбекистана и открыли реестр зарегистрированных зарубежных лекарственных средств. Эупенты там нет. Мы пробовали найти и на русском и на английском – нет ее! Как и в принципе нет ни одной корейской вакцины, как и самой компании LG Chem», – пишет журналист.
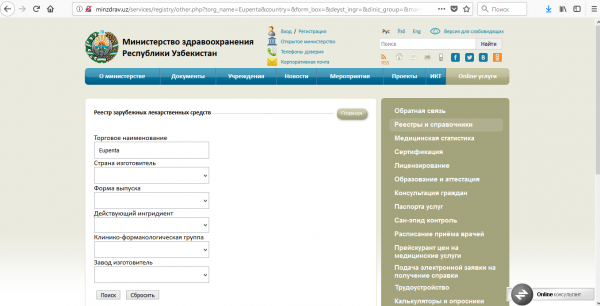
Но журналист указывает на один нюанс. «Дело в том, что в этой стране и ранее были довольно либеральные требования при регистрации лекарственных средств (в Беларуси куда жестче), а 26 июня 2018 года президент страны подписал указ №УП-5460 «О мерах по повышению эффективности государственной регистрации лекарственных средств и улучшению обеспечения ими населения». Этим документом в страну начали автоматически получать допуск все лекарственные средства, которые зарегистрированы в странах с высокими регуляторными требованиями, а также в международных организациях, чей авторитет не вызывает сомнений. ВОЗ, само собой, вошла в этот список. Поэтому Эупента, со своей преквалификацией ВОЗ просто автоматически получила доступ в Узбекистан, как и в африканские и азиатские страны, которыми козыряют корейцы. Может именно эту «регистрацию» они и имели ввиду?» – спрашивает журналист.
В Филиппинах на соответствующем сайте Департамента здравоохранения никакой информации об Эупенте нет.
В заключение «Ежедневник» говорит, что «это далеко не все сведения, которыми мы обладаем относительно вакцины Эупента. Но все же пока воздержимся от их опубликования. Вместо этого мы предлагаем компании LG Chem и Министерству здравоохранения Беларуси не публиковать ничем не подтвержденные утверждения, а предоставить беларуской общественности все имеющиеся сертификаты и регистрации, в том числе и Протокол обследования завода в Osong, проведенного после начала 2016 года. Не просто сказать, что они есть, а именно показать их».